
如期所至,ESMO大会后不足半月,FAST-TIL注册I期临床试验数据便在持续的随访中得到更新,1例PR和1例SD受试者转化为CR和PR疗效,CRR20%,ORR达到50%!中位随访已超过5.5个月,mPFS仍未达到!更高的深度缓解率显示出FAST-TIL强劲的体内持续杀伤肿瘤能力。
近期,华赛伯曼在2025 ESMO大会公布了FAST-TIL注册I期临床试验数据。创新设计带来的全封闭自动化培养体系、更少的肿瘤组织需求、更短的生产时间、更少的IL-2用量有效克服目前TIL细胞治疗技术的产业化痛点。FAST-TIL注册I期临床不断展现出的高比例深度缓解(Deepened Response)数据标志着华赛伯曼TIL的创新实现了从CMC到临床的闭环,临床疗效得到验证。
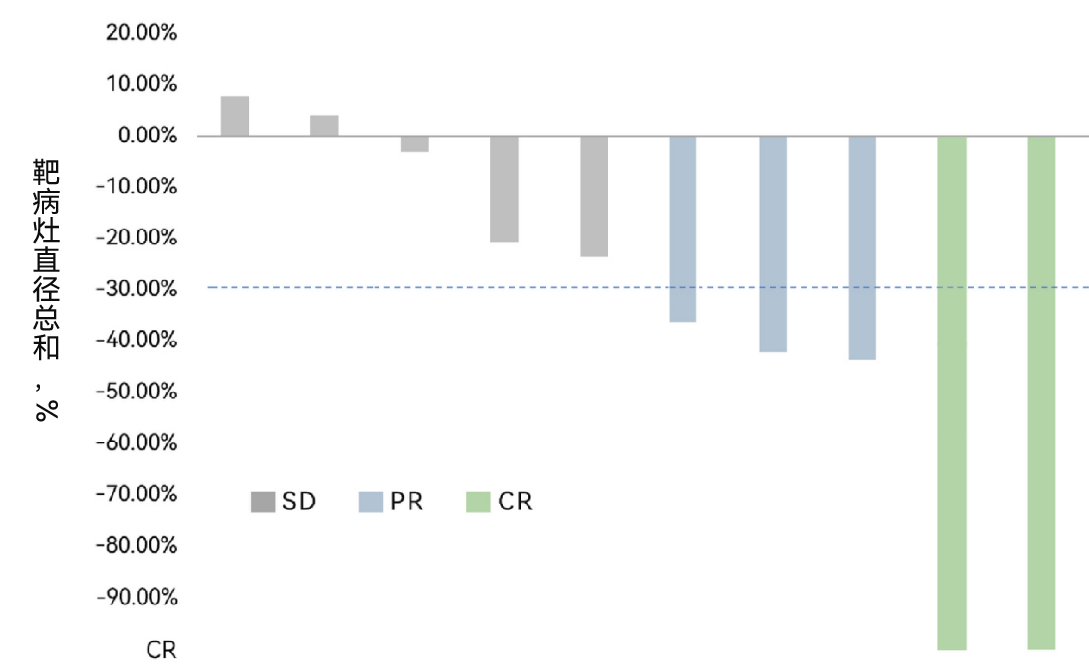
FAST-TIL疗效更新
创新设计破局TIL产业困境
2024年美国首款TIL细胞治疗药物AMTAGVI获批上市,将“实体肿瘤一针治愈”的希望变成了现实。尽管该产品使众多无药可医的晚期黑色素瘤患者通过一次性治疗实现了“肿瘤治愈”,但费用高,取材难,毒副反应大和制备周期长等问题严重限制了其上市后的临床应用。
华赛伯曼在TIL开发之初便未选择常见“跟随”模式,针对传统TIL痛点进行创新设计,经过持续的探索和打磨,成功推出了成本更低、肿瘤组织用量更少、生产更快、更低IL-2用量和临床安全性更好的FAST-TIL产品!这些特点将在未来TIL产业化中展现出巨大优势,极大提升TIL产品的可及性,使得疗效更优价格更低的TIL细胞治疗产品惠及更多实体肿瘤患者。
深度疾病缓解持续刷新疗效数据
华赛伯曼在2025 AACR大会上披露的工艺和质量数据已经显示了FAST-TIL显著优于传统TIL的产品特性。高干性和低耗竭的制剂组成预示了FAST-TIL在体内更持久的存续能力,这对于长久的疗效维持至关重要。注册I期临床试验数据同样验证了这一特点的疗效优势。在持续的疗效随访中,2例受试者SD转变为PR,1例受试者PR转为CR。最长随访的受试者治疗后一年半,病灶仍在持续缩小。多数患者在治疗后取得了更高深度疾病缓解的疗效,这预示着更长久的生存获益。目前FAST-TIL注册I期临床试验中位随访已超过5.5个月,mPFS仍未达到。基于FAST-TIL的产品特性,疗效数据将在后续随访中继续刷新!
FAST-TIL研究中心
北京大学肿瘤医院(北京)
广东省人民医院(广州)
首都医科大学附属北京市胸科医院(北京)
南昌大学第二附属医院(南昌)
北京高博医院(北京)
中国医学科学院肿瘤医院(北京)
吉林大学第一医院(长春)
四川大学华西医院(成都)
福建省肿瘤医院(福州)
✱ 公司特别声明,本新闻公告旨在发布研发临床进展信息及医药前沿信息,仅供医疗卫生专业人士参阅,非广告用途,本公司不对任何未经批准的药品和/或适应症作推荐。



