
美国当地时间2025年8月18日,全球TIL细胞药物龙头企业Iovance宣布,首款TIL细胞治疗产品Amtagvi获得加拿大联邦政府药品监管机构Health Canada批准上市,用于治疗抗PD-1治疗疾病进展(若BRAF V600突变阳性,则需接受BRAF抑制剂治疗),且没有理想的替代治疗方案的无法切除或转移性黑色素瘤成年患者。此次获批基于加拿大Notice of Compliance with Conditions (有条件批准通知,NOC/c) 指导,是Amtagvi在海外的首次获批,标志着Iovance向前迈出了重要一步,也是近期Iovance和TIL行业的又一利好信息。

收入增长稳定
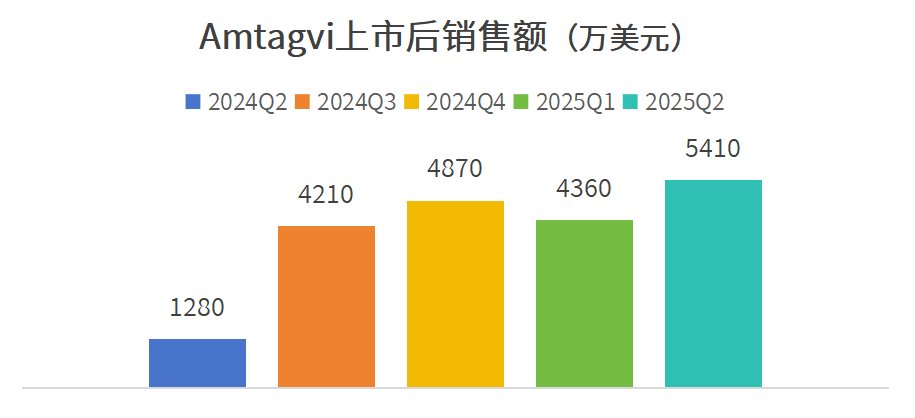
2025年因Iovance细胞治疗中心(iCTC)维护导致产能下降,Amtagvi第一季度销售额出现下滑。但Iovance 2025年第二季度及上半年财报显示,经过调整,Amtagvi第二季度销售额增长至5410万美元,维持了自去年第二季度以来的增长趋势,显示了不断扩大的市场需求。
真实世界疗效优异
2025年7月Iovance公布的4家授权治疗中心的41名患者的真实世界数据显示出优于关键临床试验阶段的疗效数据(总体ORR为48%(20/41),早期患者(既往≤2线治疗)ORR高达60.9%(14/23)),带给了大家更大的鼓舞。
海外扩张持续
在加拿大的获批是Amtagvi全球推广的第一步,Iovance将在未来几个月内授权在加拿大的细胞治疗中心,并继续推进Amtagvi在其他市场的战略。Amtagvi在欧盟的上市许可申请(MAA)正在与欧洲药品管理局(EMA)沟通中,同时有望在2026年上半年在英国和澳大利亚获批上市,将于2025年第四季度向瑞士监管机构提交优先审查申请。
尽管Iovance在年初下调了2025全年的产品指导收入,但恢复的销售增长趋势、出色的真实世界疗效数据和不断扩张的海外市场给予了大家信心与希望。虽然仍有未解决的诸多痛点,但首款TIL治疗产品仍显示出良好的增长势头,正向全球更广泛的区域推广,并解决实体瘤治疗领域更大的未被满足的需求。同时,诸多TIL开发的“新晋势力”通过不断创新解决着传统TIL的一个个痛点与短板。生产更快、成本更低、安全性更好、疗效更优的TIL产品呼之欲出。由TIL引领的实体肿瘤治疗新未来正在到来。
✱ 公司特别声明,本新闻公告旨在发布研发临床进展信息及医药前沿信息,仅供医疗卫生专业人士参阅,非广告用途,本公司不对任何未经批准的药品和/或适应症作推荐。


